NY/T 547-2002兔粘液瘤病琼脂凝胶免疫扩散试验方法
前 言
兔粘液瘤是兔的病毒性致死性传染病,世界动物卫生组织[World Organization for Animal Health(英),Office Intentional des Epizootic(法),OIE]和我国分别将之列为B类或二类动物疫病。
本标准是依据OIE 《诊断试验和疫苗标准手册》(2000版)(“Manual of Standards for DiagnosticTests and Vaccines”,2000)第2.2.1章制定的。本标准与该章的差异是:
——本标准只采用了该章规定的最实用的抗体抗原兼测的琼脂凝胶免疫扩散试验(液体法)技术,此项技术已可满足我国对内和对外诊断及检疫的需要;
——本标准基于该章的原则性规定,根据我国的研究与实践经验规定了具体的操作程序。
本标准的附录A为规范性附录。
本标准由农业部畜牧兽医局提出。
本标准由全国动物检疫标准化技术委员会归口。
本标准起草单位:农业部动物检疫所。
本标准主要起草人:杜元钊、朱万光、刘佩兰、吴延功。
1 范围
本标准规定了兔粘液瘤病琼脂凝胶免疫扩散试验的技术要求。
本标准适用于兔粘液瘤病毒特异抗体和可溶性抗原的检测,也可用于兔粘液瘤病的流行病学调查。
2 检验方法
2.1 材料
2.1.1 器材与试剂:
a) 打孔器:内径6 mm;
b) 琼脂糖:
c) 三羟甲基氨基甲烷(Tris);
d) 10%盐酸;
e) 乙二胺四乙酸(EDTA)。
2.1.2 琼脂扩散抗原,按说明书使用。
2.1.3 标准阳性血清,按说明书使用。
2.1.4 被检血清:按常规方法采血分离血清,4℃保存10d内检测有效;-20℃冻结保存,一年有效。
2.1.5 琼脂糖平板制备方法见附录A。
2.2 操作方法
2.2.1 在琼脂糖平皿上,按坐标纸上画好的梅花型(见图1)打孔,其孔径为6 mm,孔距为4 mm;孔内琼脂糖用针头小心挑出,勿破坏周围琼脂。打孔后用酒精灯加热封底。
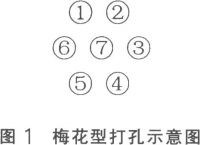
2.2.2 加样:滴加抗原和血清于梅花型孔中,中央孔(7孔)加抗原(Ag),1、3、5孔加标准阳性血清,2、4、6孔加被检血清,每孔均以加满不溢出为度。
2.2.3 反应:加样完毕后,静置10 min,然后放入带盖的湿盒中置37℃反应,24 h观察结果,48 h判定结果。阴性或可疑的结果于72h再判定一次。
2.3 结果判定
2.3.1 判定标准
检测血清中可溶性抗原或抗体出现的沉淀线:
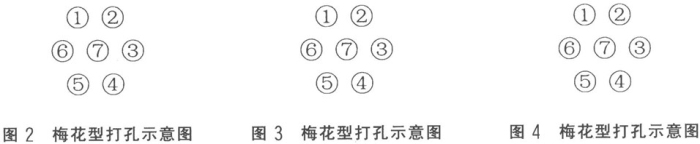
a) 如被检血清中含有可溶性抗原,则被检血清与阳性血清之间形成沉淀线,并与阳性血清和抗原形成的沉淀线交联(见图2)。
b) 如被检血清中含有抗体,则被检血清与抗原之间形成沉淀线,并与阳性血清和抗原形成的沉淀线交联(见图3)。
c) 如被检血清中同时含有可溶性抗原和抗体,则出现两条沉淀线,一条是被检血清与阳性血清之间形成沉淀线,并与阳性血清和抗原形成的沉淀线交联,第二条是待检血清与抗原之间形成沉淀线,并与阳性血清和抗原形成的沉淀线交联(见图4)。
抗体和抗原检测结果判定一样,出现清晰沉淀线,并与阳性参考血清沉淀线完全融合为阳性。
2.3.2 判定
2.3.2.1 阳性:“+”,抗原孔和血清孔之间有沉淀线。
2.3.2.2 可疑:“±”,阳性参考血清末端形成的沉淀线在被检血清处稍弯,复检仍为可疑时,判为阳性,其中弯向中央孔者为含抗体阳性;弯向周边孔者为抗原阳性。
2.3.2.3 阴性:“一”,表示被检血清孔和阳性血清孔之间无沉淀线,阳性参考血清形成的沉淀线直伸到被检血清孔的边缘。
2.3.2.4 非特异反应:被检血清虽形成沉淀线,但与阳性参考血清的沉淀线末端交叉或不相融合,该血清应判为阴性。
附录 A
附 录 A (规范性附录) 琼脂糖凝胶的配制A.1 琼脂糖凝胶配方 琼脂糖 1.0g
Tris 1.21g
氯化钠(NaCl) 5.84g
EDTA 0.372 g
蒸馏水 100mL
A.2 琼脂糖凝胶的制备 将上述各种试剂混合后加热充分溶解,用盐酸调pH值为7.4。分装刻度试管中塞紧后4℃保存,使用时熔化后浇在平皿中,有效期2个月。
A.3 平板制作 将充分熔化的琼脂糖凝胶冷却至50℃~60℃后,倒入直径9 cm的平皿中,每平皿15 mL~20 mL。注意不要产生气泡,平皿须放在平台上,待凝胶凝固后即可使用。现用现制。

